Et si vous pouviez sculpter votre propre microbiote intestinal en quelques clics ?
C’est exactement ce que propose GutQuest — un serious game pédagogique entièrement gratuit, jouable dans votre navigateur, qui transforme votre côlon en écosystème vivant à explorer, à nourrir et à soigner. Ni jeu d’arcade, ni quiz, ni infographie animée : GutQuest est une simulation écologique où chaque intervention alimentaire, médicamenteuse ou de mode de vie déclenche une cascade de réactions biologiques réalistes parmi douze espèces microbiennes modélisées.
Conçu pour un double niveau de lecture — grand public curieux et professionnels de santé —, il rend tangibles des mécanismes qui restent souvent abstraits dans les consultations : la chute de diversité après un antibiotique, la montée du butyrate grâce aux légumineuses, le rôle protecteur d’Akkermansia muciniphila dans la couche de mucus. En quelques tours de jeu, on comprend pourquoi le microbiote n’est pas un simple supplément à avaler, mais un jardin invisible qu’on cultive jour après jour.
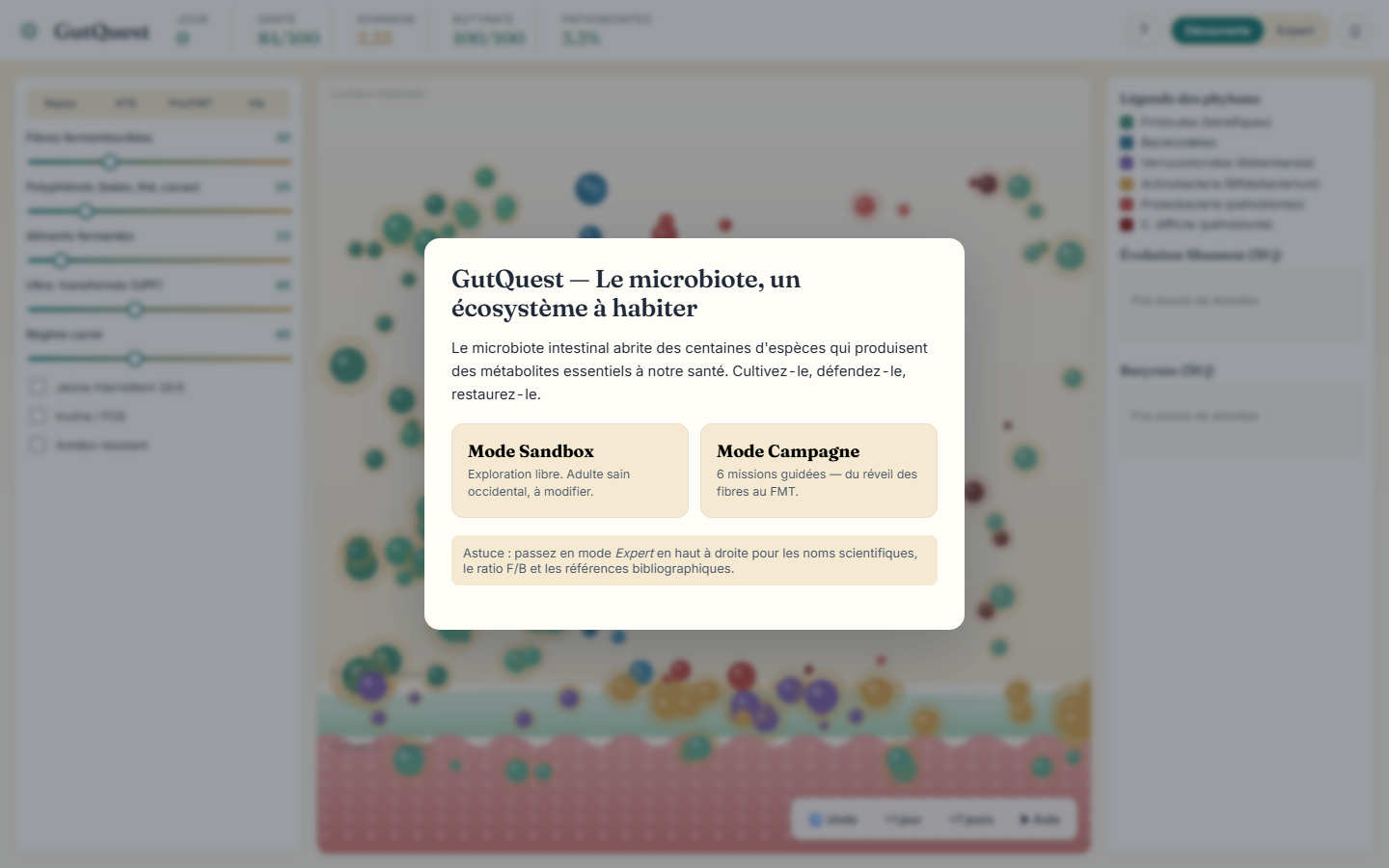
Commencez par explorer le jeu directement ci-dessous, ou ouvrez-le en plein écran pour une expérience optimale :
Le pitch : un écosystème à habiter, pas un boss à vaincre
GutQuest modélise l’intérieur d’un côlon humain comme un écosystème à trois zones, inspiré de l’anatomie réelle :
- La lumière intestinale — zone centrale, riche en substrats fermentescibles, où s’activent Bacteroides, Prevotella et Faecalibacterium prausnitzii.
- La couche de mucus — niche protectrice tapissée de glycoprotéines, domaine de prédilection d’Akkermansia muciniphila et de Bifidobacterium.
- Les cryptes, proches de l’épithélium — environnement microaérophile en contact direct avec les cellules immunitaires, occupé par Lactobacillus et certains Clostridia.
Douze espèces ou genres sont modélisés, chacun avec ses substrats préférés, ses produits métaboliques et son rôle écologique :
Les bénéfiques clés : Faecalibacterium prausnitzii, Roseburia intestinalis et Eubacterium rectale — trio producteur de butyrate, acide gras à chaîne courte (SCFA) qui nourrit les colonocytes et scelle la barrière épithéliale. Akkermansia muciniphila — gardienne du mucus, associée à la protection métabolique. Bifidobacterium — spécialiste des fibres prébiotiques (FOS, inuline, GOS). Lactobacillus — producteur de lactate, pilier des aliments fermentés.
Les commensaux ambivalents : Bacteroides et Prevotella colonisent la lumière selon le régime (occidental vs végétal). Escherichia coli commensal et Enterococcus restent discrets en bonne santé, mais basculent en pathobiontes lors d’une dysbiose.
Les pathobiontes : Clostridioides difficile, redoutée des cliniciens, et Klebsiella / Enterobacteriaceae, pro-inflammatoire — deux espèces qui explosent dans les niches libérées par les antibiotiques.
Ce n’est pas une métaphore décorative : le moteur de simulation calcule à chaque « jour » simulé la croissance de chaque espèce selon la disponibilité en substrats, la compétition pour l’espace, l’adéquation à sa niche et les modificateurs d’intervention. L’ensemble est soumis à une capacité de charge globale — le total des populations reste approximativement constant, comme dans un vrai écosystème. Quand une espèce progresse, une autre recule.
Comment ça marche : les leviers à votre disposition
Le panneau d’interventions, à gauche de la vue écosystème, regroupe quatre familles d’actions. Chaque choix se répercute immédiatement sur les populations microbiennes et sur les indicateurs de santé du tableau de bord.
Alimentation
C’est le levier le plus puissant — et le plus quotidien. Augmenter les fibres fermentescibles (légumineuses, avoine, légumes racines) fait bondir Faecalibacterium, Roseburia et Eubacterium, et avec eux la production de butyrate. Les polyphénols (baies, thé vert, cacao, huile d’olive) stimulent Akkermansia et Bifidobacterium. Les aliments fermentés (yaourt, kéfir, choucroute, kimchi) apportent un boost transitoire à Lactobacillus. À l’inverse, les ultra-transformés (UPF) effondrent la diversité, élèvent les Enterobacteriaceae et amincissent la couche de mucus — visible à l’écran. Le jeûne intermittent en 16:8 offre une fenêtre à Akkermansia, qui broute la mucine en l’absence de substrats luminaux. Les prébiotiques ciblés (inuline, FOS, amidon résistant) permettent de nourrir sélectivement les espèces souhaitées.
Antibiothérapie
C’est le levier le plus spectaculaire — et le plus risqué. GutQuest permet de choisir la molécule (amoxicilline, amoxicilline-clavulanate, ciprofloxacine, clindamycine, vancomycine orale, métronidazole), le spectre (étroit ou large) et la durée (3, 7 ou 14 jours). La clindamycine, par exemple, décime les anaérobies et ouvre une fenêtre de colonisation à C. difficile que même une alimentation riche ne referme pas immédiatement. La résilience post-antibiotique est modélisée : le microbiote peut récupérer partiellement en 1 à 3 mois avec un régime riche en fibres — mais souvent jamais complètement sans intervention active.
Probiotiques, prébiotiques et transplantation fécale (FMT)
Les probiotiques (Lactobacillus / Bifidobacterium) produisent un boost transitoire de J0 à J14, avec une réimplantation limitée. Saccharomyces boulardii offre une protection spécifique contre C. difficile pendant l’antibiothérapie. Les prébiotiques (inuline, GOS, PHGG) nourrissent les espèces bénéfiques déjà présentes — effet plus durable. La transplantation fécale (FMT) est le levier le plus radical : elle réinitialise la diversité en profondeur, avec une indication officielle dans la colite à C. difficile récidivante.
Mode de vie
Le stress chronique (cortisol élevé) réduit Lactobacillus et augmente la perméabilité intestinale. Un sommeil inférieur à 6 heures perturbe la chronobiologie microbienne et fait chuter la diversité. À l’inverse, l’exercice physique modéré et régulier est l’un des rares facteurs qui augmente spontanément Akkermansia et la production de butyrate. Les voyages en zone tropicale simulent le risque de colonisation par des bactéries multirésistantes.
Les indicateurs : ce que lit le tableau de bord
Cinq métriques principales s’affichent en temps réel dans le HUD :
- Diversité α (indice de Shannon H’) — mesure la richesse et l’équitabilité de l’écosystème, affiché de 0 à 4. Un Shannon > 3 est le signe d’un microbiote robuste.
- Production de butyrate — agrégat des populations productrices de SCFA, noté de 0 à 100.
- Charge en pathobiontes — pourcentage du total que représentent les espèces à risque. Au-delà de 15 %, la barrière commence à souffrir.
- Intégrité de la barrière — fonction d’Akkermansia, de Bifidobacterium et du butyrate. Visible à l’écran par l’épaisseur de la couche de mucus.
- Score Santé global (0–100) — composite pondéré : diversité (25 %), butyrate (20 %), barrière (20 %), absence de pathobiontes (15 %), richesse spécifique (10 %), équilibre Firmicutes/Bacteroidetes (10 %).
Deux niveaux de lecture, un seul jeu
Un interrupteur en haut à droite bascule entre deux modes qui cohabitent dans la même simulation :
🌱 Mode Découverte
Vocabulaire simplifié — « bonnes bactéries », « carburant de la barrière », « jardin à cultiver ». Bulles d’aide contextuelles. Glossaire intégré pour chaque terme technique. Idéal pour le grand public, les patients, les lycéens et les étudiants en début de cursus.
🔬 Mode Expert
Noms scientifiques complets, indices de Shannon, ratio Firmicutes/Bacteroidetes, score d’inflammation. Références bibliographiques en infobulles : Sokol 2008 pour F. prausnitzii, Cammarota 2017 pour la FMT, Dethlefsen & Relman 2011 pour la résilience post-ATB, David et al. 2014 pour la plasticité du régime. Pour les professionnels de santé, étudiants en master et chercheurs.
Six missions cliniques : des scénarios ancrés dans le réel
Au-delà du mode bac à sable (exploration libre sans objectif), GutQuest propose six missions narratives progressives :
- Le réveil des fibres (Découverte) — Microbiote appauvri par des années d’ultra-transformés. Objectif : faire grimper le butyrate au-dessus de 60/100 en trente jours simulés, en introduisant progressivement légumineuses, avoine et légumes racines. Apprentissage fondamental : fibres → SCFA → barrière.
- Antibio sous contrôle — Un patient atteint de pneumonie a besoin d’antibiotiques. À vous de choisir la molécule, la durée et la supplémentation associée pour guérir l’infection tout en maintenant un Shannon > 2,5. Mission clé pour comprendre le bon usage des ATB et le rôle protecteur de S. boulardii.
- Sauver M. D. du C. difficile (Expert) — Troisième récidive de colite après trois cures d’antibiotiques. Vancomycine longue ? Fidaxomicine ? Ou transplantation fécale ? Mission centrée sur l’indication de la FMT et la dynamique des niches libérées.
- Le marathonien — Un athlète prépare un marathon. Optimiser le microbiote pour l’endurance et la récupération musculaire, en favorisant Akkermansia et les producteurs de SCFA. Introduction à l’axe microbiote-performance sportive.
- Voyage en zone tropicale — Risque de turista et de colonisation par des bactéries multirésistantes (BMR). Stratégies de prévention avant, pendant et après le voyage, et décolonisation au retour.
- Reset après burnout (Expert) — Deux ans de stress chronique, alimentation dégradée, sommeil inférieur à cinq heures par nuit. Plan multimodal sur quatre-vingt-dix jours pour reconstruire l’écosystème. Mission la plus complexe, centrée sur l’axe intestin-cerveau et la multifactorialité des dysbioses.
🩺 Pour les professionnels de santé
GutQuest n’est pas un dispositif médical — c’est un outil pédagogique. Mais il peut changer la texture de vos consultations.
En support de discussion patient : « Regardez ce qui se passe quand on prend de la clindamycine sans probiotique protecteur. » Montrer l’animation en temps réel est souvent plus percutant que dix minutes d’explications verbales. Le jeu peut tourner en partage d’écran pendant une consultation ou être mis à disposition en salle d’attente sur une tablette.
En formation initiale et continue : Les missions « Antibio sous contrôle » et « Sauver M. D. du C. difficile » constituent des cas cliniques interactifs directement exploitables en travaux dirigés de pharmacologie ou de gastroentérologie. Le mode Expert avec ses références bibliographiques en infobulles (Sokol, Cammarota, Dethlefsen, David) s’adresse aux internes, résidents et praticiens en formation continue.
Clarté déontologique : GutQuest ne délivre aucune recommandation thérapeutique personnalisée. Il modélise des tendances de population cohérentes avec la littérature, pas des trajectoires individuelles. Il ne remplace pas un avis médical, un bilan microbiologique ni une consultation diététique spécialisée.
À retenir
- Modèle simplifié mais cohérent — 12 espèces, 3 niches, paramètres calibrés sur la littérature scientifique (Sonnenburg, Zhernakova, Rinninella, Wu…). Pas une simulation physiologique complète, mais une représentation fonctionnellement fidèle des grandes dynamiques.
- 100 % open source — code source disponible sur GitHub, ouvert aux contributions, signalements de bugs et forks pédagogiques.
- Hébergé sur GitHub Pages — aucune installation, aucune collecte de données, pas de compte requis. Chaque partie commence avec un microbiote neutre.
- Navigable sur desktop et mobile — le mode plein écran est recommandé sur mobile pour une expérience optimale du panneau d’interventions.
- Accès totalement libre — pas de paywall, pas de publicité, pas de freemium. Un outil pédagogique du bien commun numérique.
Limites et honnêteté scientifique
GutQuest est un modèle didactique, pas une simulation physiologique de précision. Ses paramètres sont calibrés sur la littérature microbiologique des quinze dernières années, mais ils sont nécessairement simplifiés : douze espèces ne capturent pas les 200 à 1 000 phylotypes que compte un microbiote adulte réel ; les dynamiques de colonisation locale varient enormément d’un individu à l’autre ; les effets d’un probiotique en simulation sont des tendances moyennes, pas des prédictions personnalisées.
En particulier : GutQuest ne constitue pas une « prescription microbiotique ». Tirer d’une partie de jeu la conclusion qu’il faudrait prendre tel prébiotique ou éviter tel antibiotique dans une situation clinique réelle serait une erreur de méthode. La simulation est là pour illustrer des mécanismes généraux, pas pour remplacer un bilan biologique, une consultation médicale ou un suivi diététique spécialisé.
Ce qui rend GutQuest utile, c’est précisément sa franchise sur ces limites : chaque indicateur est expliqué, chaque simplification est assumée, et les références scientifiques en mode Expert permettent à chacun de remonter aux sources primaires.
Code source ouvert
GutQuest est développé en HTML5 Canvas 2D et JavaScript vanilla (pas de framework, pas d’asset binaire externe — tout est dessiné par code). Le jeu est entièrement ouvert sur GitHub. Pull requests et signalements de bugs bienvenus — qu’il s’agisse d’améliorer la modélisation d’une espèce, d’ajouter une langue, de corriger une traduction ou de proposer une nouvelle mission clinique.
🇬🇧 Read this article in English: GutQuest — explore your gut microbiome as a 2D ecosystem
NutriCellScience, Mark DOWN
Laisser un commentaire