La grippe espagnole de 1918. Le SARS de 2003. La pandémie H1N1 de 2009. Ebola. Le SARS-CoV-2 de 2020. Ces cinq catastrophes sanitaires mondiales ont un point commun : elles sont toutes causées par des virus à ARN. Coïncidence ? Non — biologie moléculaire. Les virus à ARN mutent 10 000 fois plus vite que leurs cousins à ADN, selon une méta-analyse fondatrice de Sanjuán et collègues (2010). Cette vitesse d’évolution inouïe leur confère une capacité d’adaptation permanente qui fait le lit des pandémies. Mais la réalité est plus nuancée : les virus à ADN ne sont pas inoffensifs pour autant — ils ont développé d’autres stratégies, tout aussi redoutables.
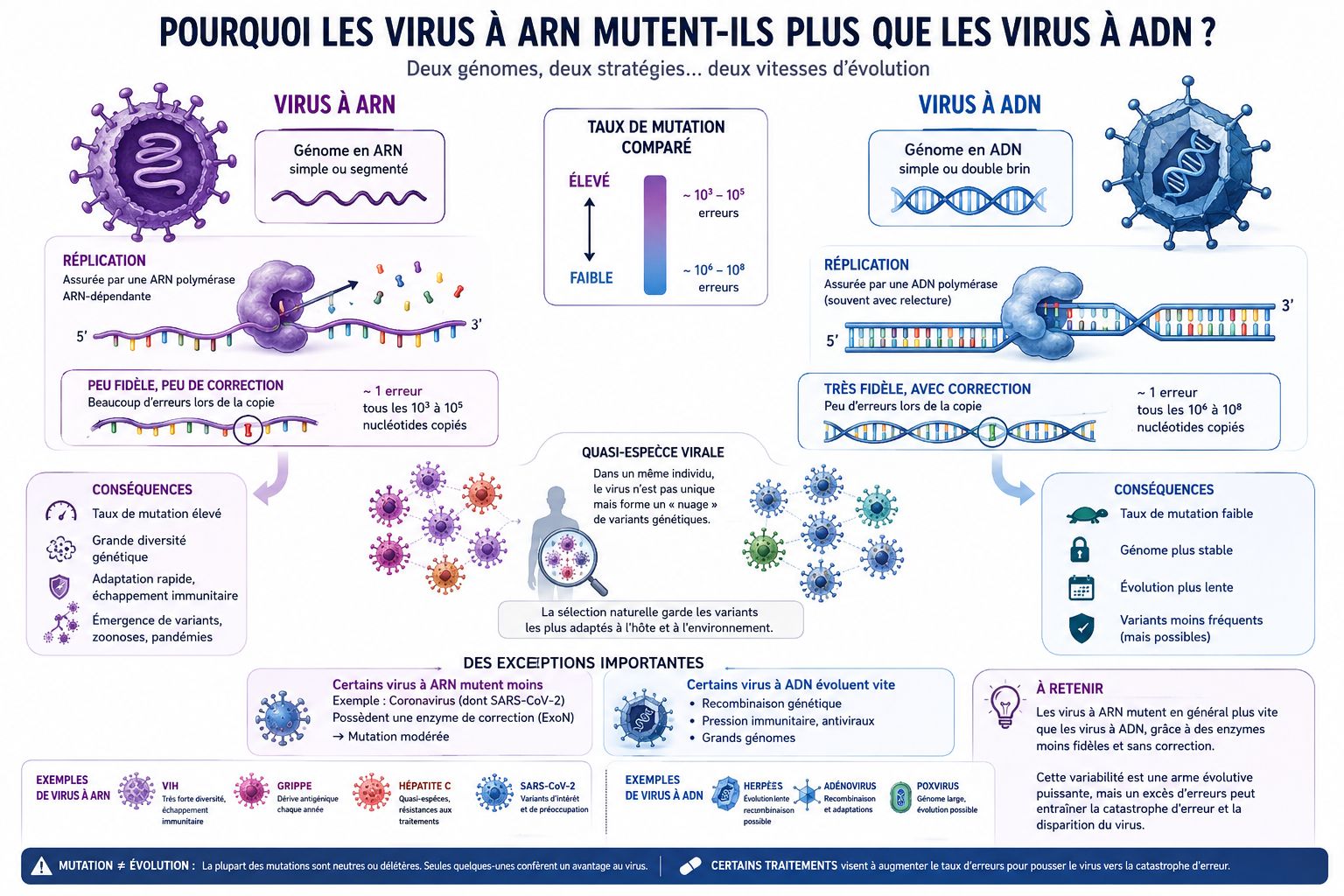
1. La leçon des chiffres : pourquoi les virus ARN mutent autant
Commençons par les données brutes. Dans une méta-analyse publiée en 2010 dans le Journal of Virology, Sanjuán et collègues ont compilé plus de quarante études portant sur vingt-trois virus différents. Résultat : les virus à ARN présentent des taux de mutation compris entre 10⁻⁶ et 10⁻⁴ substitutions par nucléotide et par cycle d’infection, avec une valeur centrale autour de 2,2 × 10⁻⁵. Les virus à ADN, eux, se situent entre 10⁻⁸ et 10⁻⁶. Il n’y a aucun chevauchement entre les deux distributions — un fossé de plusieurs ordres de grandeur sépare les deux groupes.
Pour rendre ces chiffres concrets : influenza A accumule 2,3 × 10⁻⁵ mutations par nucléotide et par infection ; le VHC atteint 1,2 × 10⁻⁴ ; à l’opposé, l’herpès simplex HSV-1 ne mute qu’à 5,9 × 10⁻⁸ — soit 4 à 5 ordres de grandeur de moins. Une revue d’Esteve Domingo et collègues (Viruses, 2021) confirme que les virus ARN mutent « un ou plusieurs ordres de grandeur au-dessus de la réplication de l’ADN cellulaire ».
Chaque fois qu’un virus ARN se reproduit, il produit des copies légèrement différentes. Certaines disparaîtront. D’autres disposeront d’une mutation favorable : une protéine qui échappe aux anticorps, une polymérase plus rapide, une résistance aux antiviraux. C’est l’évolution darwinienne à l’accéléré.
2. Le proofreading : l’arme moléculaire des virus à ADN
Pourquoi cette différence abyssale ? La réponse tient en un mot : proofreading — que l’on peut traduire par « relecture de l’imprimerie ». Imaginez un typographe qui, après avoir composé une page, la relit méticuleusement avant impression pour corriger chaque coquille. C’est exactement ce que font les ADN polymérases des virus à ADN grâce à leur activité exonucléasique 3’→5′ : elles relisent le brin nouvellement synthétisé, détectent les nucléotides mal incorporés et les excisent avant de les remplacer par les bons.
Les ARN polymérases (RdRp, pour RNA-dependent RNA polymerase) des virus à ARN n’ont pas cette capacité de relecture. Comme le soulignent Carrasco-Hernández et collègues dans l’ILAR Journal de 2017, « l’absence d’activité exonucléasique augmente le taux de mutation ponctuelle du génome en omettant la correction d’erreurs pendant la réplication ». Résultat : chaque copie accumulera plusieurs erreurs non corrigées, qui s’accumuleront génération après génération.
Mais il existe une exception remarquable : les coronavirus. Ces virus ARN à brin positif sont les seuls à posséder une machinerie de proofreading fonctionnelle — l’exonucléase nsp14-ExoN. Smith et Denison ont décrit ce mécanisme dans un article conceptuel marquant de PLOS Pathogens en 2013, avec un titre délibérément provocateur : « Les coronavirus comme virus à ADN en devenir ». Cette exonucléase leur permet de maintenir un génome de 26 à 32 kilobases — le plus grand de tous les virus ARN à brin simple —, alors que les autres virus ARN sont contraints à 9–14 kb sans capacité de correction. Le VIH n’a que ~9 kb ; le virus grippal, ~14 kb segmentés ; le VHC, ~9,6 kb.
Les travaux de Subissi et collègues, publiés dans PNAS en 2014, ont cartographié pour la première fois le complexe intégré nsp7-nsp8-nsp12 (la polymérase) + nsp14-ExoN : polymérase et exonucléase fonctionnent ensemble, comme un tandem de haute fidélité. Une autre étude de Smith et collègues (2013) dans PLOS Pathogens a démontré expérimentalement que des coronavirus privés de leur ExoN (ExoN⁻) accumulaient 15 à 20 fois plus de mutations que la souche sauvage, et devenaient jusqu’à 300 fois plus sensibles à la ribavirine — un analogue nucléosidique mutagène. La résistance naturelle du SARS-CoV-2 aux antiviraux de première génération s’explique en grande partie par ce mécanisme.
3. La théorie des quasi-espèces : le virus comme nuage mutationnel
Pour comprendre la dynamique évolutive des virus ARN, il faut franchir un pas conceptuel : un virus ARN n’est pas une entité unique, mais un essaim — un nuage de variants génétiques légèrement différents les uns des autres, gravitant autour d’une séquence consensus. C’est la théorie des quasi-espèces, formalisée par le Prix Nobel de chimie Manfred Eigen dès les années 1970 et développée depuis par Esteve Domingo, l’un des grands noms de la virologie des ARN.
Dans un article fondateur de PNAS en 2002, Eigen a formalisé ce que l’on appelle la catastrophe d’erreur (error catastrophe) : si le taux de mutation d’un virus ARN dépasse un seuil critique, l’information génétique se dilue jusqu’à devenir incohérente — le virus perd sa capacité à se reproduire et s’éteint. C’est une limite thermodynamique à l’évolution virale. Sanjuán (2012) dans PLOS Pathogens a quantifié cette frontière : « Une simple multiplication par trois du taux de mutation peut entraîner des pertes de fitness drastiques chez les virus ARN à brin simple. »
Ce concept a une conséquence thérapeutique directe : si l’on peut pousser un virus ARN au-delà de ce seuil d’erreur en augmentant artificiellement son taux de mutation, on peut le tuer. C’est la logique de la mutagenèse létale. Hadj Hassine, Ben M’hadheb et Menéndez-Arias ont fait le point sur cette stratégie dans Viruses en 2022 : plusieurs antiviraux approuvés exploitent ce mécanisme.
- Ribavirine : analogue nucléosidique utilisé contre le VHC, la fièvre de Lassa et d’autres infections à virus ARN ; augmente le taux de mutation viral.
- Favipiravir : s’incorpore à l’ARN viral et provoque des transitions G→A et C→U, surchargeant la machinerie de réplication.
- Molnupiravir (prodrug de β-d-N4-hydroxycytidine) : approuvé pour le SARS-CoV-2 en 2021 ; se montre environ 100 fois plus actif que la ribavirine contre le SARS-CoV-2 dans les modèles cellulaires.
La théorie des quasi-espèces explique aussi pourquoi il est si difficile d’éradiquer le VIH : à tout moment, dans le « nuage » mutationnel qui constitue la population virale d’un patient, certains variants sont déjà résistants aux antiviraux qui n’ont pas encore été administrés. Carrasco-Hernández et collègues (2017) notent que le VIH-1 peut développer une résistance aux INNRT (inhibiteurs non nucléosidiques de la transcriptase inverse) avec une seule mutation.
4. Pourquoi presque toutes les pandémies récentes sont à virus ARN
Woolhouse et collègues ont recensé en 2012, dans les Philosophical Transactions of the Royal Society B, les 219 espèces de virus reconnues à l’époque par l’ICTV (Comité international de taxonomie des virus) comme capables d’infecter l’homme. Parmi elles, plus des deux tiers sont d’origine zoonotique — elles ont un réservoir animal non humain, principalement chez les mammifères. C’est le premier facteur de risque pandémique : un réservoir animal considérable, en contact croissant avec les populations humaines.
Le second facteur, c’est la capacité d’adaptation. Carrasco-Hernández et collègues (2017) estiment que les virus ARN représentent 25 à 44 % de toutes les maladies infectieuses émergentes selon les études, alors qu’ils ne constituent qu’une fraction de la diversité virale totale. Leur taux de mutation élevé leur permet de franchir les barrières d’espèces plus facilement que les virus à ADN : chaque cycle de réplication génère des variants qui « testent » de nouveaux récepteurs cellulaires, de nouveaux hôtes intermédiaires, de nouvelles voies de transmission.
Les grandes pandémies modernes illustrent cette dynamique sans exception :
- Grippe saisonnière et pandémique : virus ARN à génome segmenté en 8 fragments. Ce découpage permet le réassortiment — deux souches différentes qui infectent simultanément une même cellule peuvent échanger des segments entiers, créant un virus radicalement nouveau. C’est ainsi qu’ont émergé H2N2 (1957), H3N2 (1968) et H1N1 (2009).
- VIH : rétrovirus ARN avec une transcriptase inverse sujette à des erreurs massives. L’adaptation aux nouvelles thérapies se joue en quelques semaines.
- Ebola : filovirus ARN à brin négatif, taux de létalité entre 25 % et 90 % selon les épidémies.
- Zika : flavivirus ARN, responsable de microcéphalies néonatales lors de l’émergence en Amérique latine en 2015-2016.
- SARS-CoV-2 : coronavirus ARN dont le taux d’évolution in vivo est estimé à (1,2 ± 0,5) × 10⁻³ substitutions par site et par an — générant des variants (Alpha, Delta, Omicron) en quelques mois.
Keusch, Daszak et collègues, dans une revue publiée dans PNAS en 2022, confirment que toutes les grandes épidémies à virus ARN depuis 1967 partagent les mêmes facteurs : origines ancestrales chez les chauves-souris, les oiseaux ou d’autres mammifères ; hôtes intermédiaires facilitant l’adaptation ; et un déversement (spillover) vers l’homme favorisé par la dégradation des écosystèmes et le contact accru faune-bétail-humains. Ils estiment que 650 000 à 840 000 zoonoses inconnues restent encore à émerger dans le pool viral mondial.
La grippe mérite une mention particulière. Liang, dans une revue complète sur la pathogénicité d’influenza publiée dans Virulence en 2023, décrit deux mécanismes distincts d’émergence pandémique : la dérive antigénique (antigenic drift), accumulation continue de petites mutations qui rendent un vaccin progressivement moins efficace ; et le changement antigénique (antigenic shift), réassortiment brutal de segments entiers qui génère un virus pour lequel la population n’a aucune immunité préexistante. L’influenza A H5N1 et H7N9, bien que non encore adapté à la transmission interhumaine efficace, présentent des taux de létalité supérieurs à 50 % chez l’homme — un risque pandémique majeur surveillé en permanence.
5. Les virus à ADN : autres stratégies, autres dangers
Il serait trompeur de conclure que les virus à ADN sont inoffensifs. Ils ont simplement opté pour une stratégie évolutive différente : plutôt que la rapidité d’adaptation, ils misent sur la persistance et la manipulation cellulaire à long terme.
Prenons l’exemple des herpesvirus. Le HSV-1 (herpès labial), après la primo-infection, s’installe dans les ganglions nerveux et y reste à vie en état de latence — le génome viral persiste dans le noyau de la cellule hôte sans se répliquer activement, invisible au système immunitaire. À l’occasion d’un stress ou d’une immunodépression, il se réactive. Le cytomégalovirus (CMV), autre herpèsvirus à ADN, représente l’infection congénitale virale la plus fréquente dans les pays développés. Le virus d’Epstein-Barr (EBV) infecte plus de 90 % de la population mondiale et est associé à plusieurs cancers.
L’oncogenèse virale est en effet le terrain de prédilection des virus à ADN. Vojtěchová et Tachezy, dans une revue publiée dans le Journal of Virology en 2025, ont passé en revue les mécanismes d’intégration génomique de HPV, HBV, EBV et du polyomavirus de Merkel (MCV). Leur conclusion : 13 % des tumeurs mondiales sont d’origine infectieuse, et les virus ADN oncogènes représentent environ 60 % de ce sous-ensemble.
- HPV (virus du papillome humain) : les protéines virales E6 et E7 dégradent respectivement p53 (le « gardien du génome ») et pRb (une protéine suppresseur de tumeur), déclenchant une cascade d’instabilité génomique menant au cancer du col de l’utérus et d’autres carcinomes.
- HBV (hépatite B) : s’intègre dans des sites fragiles du génome humain, active des proto-oncogènes, et provoque une inflammation chronique propice à l’hépatocarcinome.
- EBV : associé au lymphome de Burkitt, au carcinome nasopharyngé et à certains lymphomes hodgkiniens.
La distinction est nette : les virus ARN menacent par leur adaptabilité rapide ; les virus ADN menacent par leur capacité à s’installer durablement et à détourner la biologie cellulaire. L’explosion pandémique d’un côté, la lente dérive carcinogène de l’autre.
🩺 Pour les professionnels de santé — Points cliniques clés
Surveillance de la grippe : le réassortiment (changement antigénique majeur) et la dérive antigénique sont deux mécanismes distincts. Le premier justifie la surveillance virale continue par les réseaux Sentinelles et l’OMS ; le second explique la mise à jour annuelle de la composition vaccinale. En pratique clinique, une primo-infection grippale ou une vaccination récente n’offre qu’une protection partielle contre un sous-type réassortant radicalement nouveau (cf. H1N1 2009). La surveillance One Health — incluant la surveillance des élevages porcins et aviaires — est le premier rempart contre l’émergence d’une souche à potentiel pandémique.
Implications vaccinales : les vaccins ARNm contre le SARS-CoV-2 ont dû être reformulés plusieurs fois (Bivalent BA.4/BA.5, XBB.1.5, JN.1) précisément en raison de la dérive génétique accélérée du virus. Ce phénomène est structurel, pas conjoncturel : tout vaccin contre un virus ARN à fort taux de mutation devra anticiper sa mise à jour régulière. Les plateformes ARNm offrent ici un avantage logistique majeur sur les vaccins classiques (délai de production réduit de mois à semaines).
Résistance antivirale : la structure quasi-espèce des virus ARN signifie que des variants résistants préexistent avant tout traitement. Pour le VIH, la trithérapie (trois antiviraux ciblant des mécanismes différents) a été conçue pour rendre statistiquement quasi-impossible l’émergence simultanée de mutations de résistance sur les trois cibles. Pour le SARS-CoV-2, le molnupiravir et le nirmatrelvir (Paxlovid) ont des profils de résistance distincts — une combinaison est à l’étude. La résistance naturelle des coronavirus à la ribavirine s’explique par leur ExoN, rappelant l’intérêt thérapeutique d’inhiber nsp14 pour « sensibiliser » le virus.
Bioسécurité One Health : l’approche One Health est le cadre recommandé par l’OMS et la FAO pour prévenir les pandémies à virus ARN. La réduction des drivers de spillover (déforestation, élevage intensif, marchés d’animaux vivants) est la priorité de prévention primaire selon Keusch et Daszak (2022). Tout cluster de pneumopathies atypiques ou syndromes hémorragiques d’étiologie incertaine doit déclencher une notification accélérée aux autorités sanitaires.
⚡ À retenir — Les 5 points essentiels
- Les virus ARN mutent ~10 000 fois plus vite que les virus ADN : taux de 10⁻⁶ à 10⁻⁴ versus 10⁻⁸ à 10⁻⁶ substitutions/nucléotide/infection, sans aucun chevauchement entre les deux groupes (Sanjuán 2010).
- La cause fondamentale : l’absence de proofreading. Les ARN polymérases ne corrigent pas leurs erreurs ; les ADN polymérases oui. Les coronavirus font exception en possédant l’exonucléase nsp14-ExoN — la seule machinerie de relecture connue chez un virus ARN.
- La théorie des quasi-espèces (Eigen, Domingo) explique comment un virus ARN existe comme un nuage de variants plutôt que comme une entité unique, rendant l’éradication et la résistance antivirale structurellement difficiles.
- Presque toutes les pandémies modernes sont ARN : grippe, SARS, MERS, Ebola, Zika, VIH, COVID-19. Les virus ARN franchissent les barrières d’espèces plus facilement et s’adaptent plus rapidement que les virus ADN (Carrasco-Hernández 2017 ; Keusch & Daszak 2022).
- Les virus ADN ne sont pas inoffensifs — ils utilisent d’autres stratégies : latence à vie (herpès), oncogenèse (HPV, HBV, EBV). 13 % des tumeurs mondiales sont d’origine infectieuse, dont ~60 % imputables à des virus ADN oncogènes (Vojtěchová & Tachezy 2025).
Bibliographie
- Sanjuán R, Nebot MR, Chirico N, Mansky LM, Belshaw R. Viral Mutation Rates. Journal of Virology. 2010;84(19):9733–9748. doi:10.1128/JVI.00694-10
- Domingo E, García-Crespo C, Lobo-Vega R, Perales C. Mutation Rates, Mutation Frequencies, and Proofreading-Repair Activities in RNA Virus Genetics. Viruses. 2021;13(9):1882. doi:10.3390/v13091882
- Sanjuán R. From Molecular Genetics to Phylodynamics: Evolutionary Relevance of Mutation Rates Across Viruses. PLOS Pathogens. 2012;8(5):e1002685. doi:10.1371/journal.ppat.1002685
- Smith EC, Denison MR. Coronaviruses as DNA Wannabes: A New Model for the Regulation of RNA Virus Replication Fidelity. PLOS Pathogens. 2013;9(12):e1003760. doi:10.1371/journal.ppat.1003760
- Smith EC, Blanc H, Vignuzzi M, Denison MR. Coronaviruses Lacking Exoribonuclease Activity Are Susceptible to Lethal Mutagenesis: Evidence for Proofreading and Potential Therapeutics. PLOS Pathogens. 2013;9(8):e1003565. doi:10.1371/journal.ppat.1003565
- Subissi L, Posthuma CC, Collet A, et al. One severe acute respiratory syndrome coronavirus protein complex integrates processive RNA polymerase and exonuclease activities. PNAS. 2014;111(37):E3900–E3909. doi:10.1073/pnas.1323705111
- Eigen M. Error catastrophe and antiviral strategy. PNAS. 2002;99(21):13374–13376. doi:10.1073/pnas.212514799
- Hadj Hassine I, Ben M’hadheb M, Menéndez-Arias L. Lethal Mutagenesis of RNA Viruses and Approved Drugs with Antiviral Mutagenic Activity. Viruses. 2022;14(4):841. doi:10.3390/v14040841
- Woolhouse MEJ, Scott F, Hudson Z, Howey R, Chase-Topping M. Human viruses: discovery and emergence. Philosophical Transactions of the Royal Society B. 2012;367(1604):2864–2871. doi:10.1098/rstb.2011.0354
- Keusch GT, Amuasi J, Anderson DE, Daszak P, et al. Pandemic origins and a One Health approach to preparedness and prevention: Solutions based on SARS-CoV-2 and other RNA viruses. PNAS. 2022;119(42):e2202871119. doi:10.1073/pnas.2202871119
- Carrasco-Hernández R, Jácome R, López Vidal Y, Ponce de León S. Are RNA Viruses Candidate Agents for the Next Global Pandemic? A Review. ILAR Journal. 2017;58(3):343–358. doi:10.1093/ilar/ilx026
- Liang Y. Pathogenicity and virulence of influenza. Virulence. 2023;14(1):2223057. doi:10.1080/21505594.2023.2223057
- Vojtěchová Z, Tachezy R. Genome integration of human DNA oncoviruses. Journal of Virology. 2025;99:e00562-25. doi:10.1128/jvi.00562-25
Article rédigé à partir d’une revue de 13 sources scientifiques vérifiées (PubMed/PMC).
🇬🇧 Read this article in English: Why are RNA viruses more dangerous than DNA viruses?
NutriCellScience, Mark DOWN
Laisser un commentaire